
Distribuição
Metabolização
Absorção
Transporte
Eliminação
ADMET
Absorção | Distribuição | Metabolização | Eliminação | Transporte
Propriedades Farmacocinéticas



Biodisponibilidade
30-60%

Clearance
15-92 L/h
Tempo de semi-vida
21h
Volume de
distribuição

2 - 12 L/Kg
Metabolitos ativos
Não tem
Absorção
[1] [2]
A nível de absorção a Paroxetina sofre metabolismo de primeira passagem, sendo bem absorvida a nível gastrointestinal. Por essa razão, apresenta uma biodisponibilidade de 30% - 60%.
A concentração máxima de Paroxetina é atingida 2h-8h após a toma do fármaco, sendo o tempo máximo médio de aproximadamente 4h. Estes tempos são determinados em indivíduos saudáveis.
7 a 4 dias após o inicio da terapêutica com Paroxetina a concentração de Paroxetina no estado de equilíbrio é atingido.
A AUC foi de 574 ng·h/mL e 1053ng·h/mL, em pacientes saudáveis e em pacientes com insuficiência renal moderada, respectivamente.

Distribuição
[1] [2]
Em função do carácter lipofílico, a Paroxetina distribui-se amplamente, sendo encontrada em todo o corpo, incluindo no sistema nervoso central. Apenas 1% do fármaco permanece no plasma.
95% da Paroxetina está ligada a proteínas plasmáticas.
Este fármaco é seguro na fase de amamentação? Sim, uma vez que a Paroxetina, para uma única dose de 50 mg, é encontrada no leite materno em concentrações na ordem dos nanogramas/mL, sendo, por isso, um fármaco seguro para mulheres em período de amamentação.

Metabolização
[1] [3] [5]
A Paroxetina é um fármaco bem absorvido no trato gastrointestinal e sofre um metabolismo de primeira passagem no fígado, originando o catecol, como produto intermediário, e metabolitos inativos. Este metabolismo é mediado pela CYP2D6 o que faz com que a cinética de eliminação da Paroxetina seja um processo saturável. No entanto, existe o envolvimento de outras isoenzimas do citocromo P450, nomeadamente, CYP 3A4 > CYP 1A2 > CYP 2C19 > CYP 3A5.
A Paroxetina é, também, um forte inibidor da CYP2D6, podendo afetar o seu próprio metabolismo.
A metabolização deste fármaco estará dependente da quantidade de CYP2D6 disponível. Sabe-se, no entanto, que em indivíduos com a atividade da CYP2D6 diminuída, terão a Paroxetina metabolizada pela CYP3A4 e a CYP1A2.
A CYP2D6 catalisa a desmetilação do grupo metilenodioxi, produzindo paroxetina-catecol, que é descrito como um intermediário instável. As enzimas catecol-O-metiltransferase (COMT) metilam o intermediário paroxetina-catecol, produzindo os metabolitos I e II. Os metabolitos I e II são encontrados como conjugados de glucuronídeo ou sulfato na urina, sendo o metabolito I o principal metabolito.

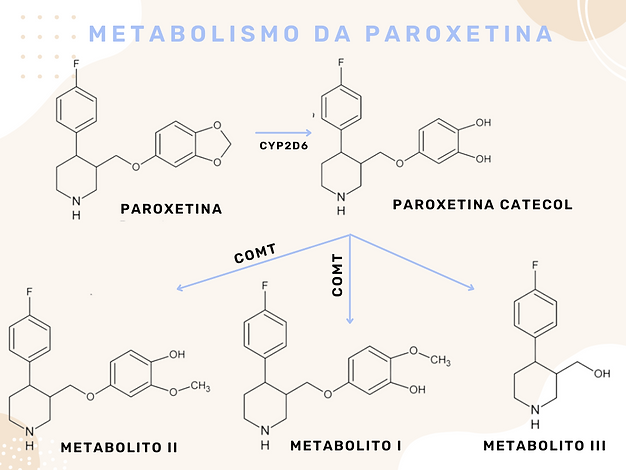
Farmacogenética
[3]
Uma consequência dos metabolizadores baixos é a acumulação do fármaco no organismo, uma vez que não existe capacidade de metabolizar a Paroxetina, justificando o aumento dos efeitos adversos. Já com os metabolizadores rápidos acontece o contrário, neste caso a concentração do limiar do fármaco não é alcançado devido à sua rápida metabolização e, consequentemente, o fármaco não exerce a sua função terapêutica.
O citocromo CYP2D6 apresenta um elevado polimorfismo, o que faz com que este citocromo apresente uma grande variabilidade no metabolismo de vários fármacos, influenciando, por exemplo, os parâmetros farmacocinéticos da Paroxetina. Podemos diferenciar os metabolizadores fracos que demonstram efeitos adversos aumentados, e os metabolizadores rápidos que, por outro lado, terão efeitos reduzidos.

Eliminação
[1] [2]
A maioria da Paroxetina (⅔ da dose inicial) é excretada na urina, sendo o restante eliminado nas fezes. A Paroxetina é eliminada sob a forma de metabolitos e cerca de 3% da dose é eliminada na sua forma ativa.

A eliminação por metabolitos é bifásica, uma vez que, inicialmente, resulta do metabolismo de primeira passagem existente no fígado e, posteriormente, é controlada por eliminação sistémica.
Possui um tempo de semi-vida de, aproximadamente, 21 horas e, apesar de variar, o facto de ser relativamente curto pode justificar o aparecimento do síndrome de abstinência, aquando uma interrupção repentina do tratamento.
Transporte
[3] [4]
A Paroxetina é um substrato de uma proteína membranar da família dos transportadores ATP- binding cassete (ABC), o transportador ABCB1.
Apesar de, ainda, não existirem estudos que demonstrem o seu envolvimento na atividade central da Paroxetina, sabe-se que devido a polimorfismos do substrato ABCB1, a função da glicoproteína-P pode ser influenciada, havendo alteração dos níveis plasmáticos dos fármacos que são substratos desta.
A glicoproteína-P expressa nas células da BHE, codificada pelo substrato ABCB1, permite a passagem de Paroxetina, a nível cerebral, por transporte ativo.
Referências Bibliográficas:
[1] DrugBank | Paroxetine. Disponível em: https://www.drugbank.ca/drugs/DB00715
[2] Infarmed | Resumo das Características do Medicamento: Seroxat 20mg comprimidos revestidos por película.
[3] Katrin Sangkuhl, Kevin Hicks, Julia Stingl. Paroxetine Pathway, Pharmacokinetics. PharmGKB. https://www.pharmgkb.org/pathway/PA166121347.
[4] Simoons M, Mulder H, Appeldoorn J, Risselada AJ, Schene AH, van Schaik R, van Roon EN, Ruhé EG (2020). Modification of the association between paroxetine serum concentration and SERT-occupancy by ABCB1 (P-glycoprotein) polymorphisms in major depressive disorder. Psychiatric genetics, 30(1):19–29. https://doi.org/10.1097/YPG.0000000000000244
[5] Jornil, J., Jensen, K. G., Larsen, F., & Linnet, K. (2009). Identification of Cytochrome P450 Isoforms Involved in the Metabolism of Paroxetine and Estimation of Their Importance for Human Paroxetine Metabolism Using a Population-Based Simulator. Drug Metabolism and Disposition, 38(3), 376–385.